Daraxonrasib第三期數據出爐 轉移性胰腺癌存活期翻倍
- Biological technology , Ai 人工智能 , 科技教育
- 2026年4月18日
Table Of Contents
超過 90% 的胰腺導管腺癌(PDAC)病例確實存在 KRAS 基因突變,KRAS 突變被認為「驅動」胰腺癌出現和發展,癌細胞能夠在惡劣腫瘤微環境中存活、瘋狂增殖和轉移。病人五年存活率,一般只有3%左右。KRAS 是人體中 RAS 基因家族成員,也可以说:胰腺癌是 RAS 信號通路依賴型的癌症。雖然發現了生物標記,長期以來,KRAS 蛋白被認為是「不可成藥」的靶點,因為其表面光滑,,開發藥物與其活化分子 GTP 競爭結合位置極其困難,難以與小分子藥物結合。KRAS 突變常見於非小細胞肺癌、大腸直腸癌及胰臟癌中,其中一種特定突變RAS-G12C,佔了相當大的比例。
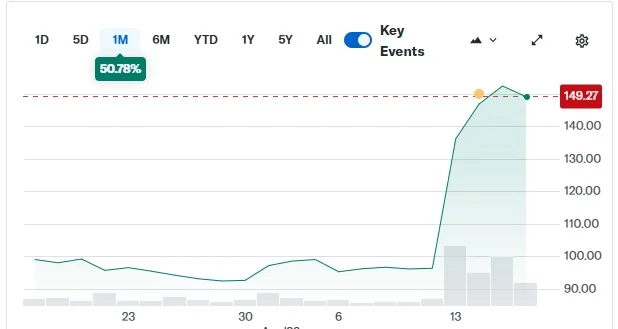
美國癌症協會最新數據顯示,轉移性的胰腺導管腺癌(PDAC)確診後,中位整體存活期竟不足七個月。Amgen(安進)在2021年獲批的Sotorasib針對了RAS-G12C,但仍然無法解決胰腺癌的G12D/G12V靶點。三月份,《新英格蘭醫學雜誌(NEJM)》發表了首款靶向KRAS G12D的蛋白降解劑Setidegrasib(ASP3082)的I期臨床研究結果。不過美國 Revolution Medicines(Ticker: RVMD, Exchange: NASDAQ)4月13日公佈全球多中心第三期試驗RASolute 302的頂線結果,口服小分子RAS(ON)多選擇性抑制劑Daraxonrasib,二線治療的整體存活期從6.7個月延長至13.2個月,風險比0.40(p<0.0001),無進展存活期(PFS)亦達統計學顯著差異,為「沉默殺手」帶來首個專門靶向RAS的治療方案。
Revolution Medicines的突破是基於哈佛大學Greg Verdine教授在2012年開發的分子膠水(molecular glue),通過「呈遞蛋白」 (presenter proteins) (類似 Cyclophilin A or FKBP12) 有如膠水將藥物黏附在類似KRAS難以附著的靶點,2012年Verdine成立了Warp Drive Bio公司,以上述技術開發出對付 KRAS 的SMART平台,2018年10月Revolution Medicines收購了Warp Drive Bio,獲得上述技術,結果成功開發出繼Sotorasib之後的廣譜藥物Daraxonrasib,可針對整個RAS家族,意義更大,而且臨床數據之佳,股價應聲向上。
RASolute 302(NCT06625320)作為一項開放標籤、隨機對照研究項目,共納入了逾400名帶有RAS G12突變的轉移性胰腺癌患者,按二比一比例分配至daraxonrasib組或研究者選擇的標準化療組作為對照,獨立中央審查評估PFS與整體存活期(OS),關鍵次要終點包括客觀緩解率(ORR)、疾病控制率(DCR)及安全性。 頂線數據顯示,daraxonrasib以300 mg每日一次口服方案在RAS G12D、G12V及G12R亞組均呈一致效益,中位PFS從2.1個月延長至5.6個月,ORR由4%提升至21%。藥物整體耐受性良好,最常見≥3級不良事件為腹瀉(11%)、疲勞(9%)及中性粒細胞減少(7%),未出現新的安全信號,亦無因治療相關死亡個案。 技術平台與分子骨架
Daraxonrasib採用「三環吡啶并嘧啶」骨架,透過自由能微擾(FEP)平台篩選,可同時佔據RAS蛋白的開關I與開關II口袋,阻斷與下游效應子RAF、PI3K的交互作用,從而抑制MAPK與PI3K/AKT/mTOR雙信號通路。相較於僅針對G12C的共價抑制劑,daraxonrasib覆蓋更廣泛的活化態RAS突變,理論上可適用於逾九成胰腺癌及約三成非小細胞肺癌。
香港癌症資料統計中心最新數據顯示,稱為「癌王」的胰臟癌有年輕化趨勢,死亡率逾8成,而且遲發現難治,胰臟癌5年存活率可低於5%,死亡率為所有主要癌症中最高。RAS(ON) 蛋白的藥物在治療KRAS G12D 突變的胰臟癌患者中表現出令人鼓舞的療效,超過90%胰腺癌患者由RAS蛋白突變引起,估計Daraxonrasib對大部分胰腺癌有效。RASolute 302臨床招募了攜帶多種RAS變異的胰腺,所以對於轉移性胰腺癌患者來說,RASolute 302臨床可算是歷史時刻。
Daraxonrasib已獲得FDA新推出的局長國家優先憑證(CNPV)——試點項目首批不可轉讓憑證,作用是大幅縮短藥物審批時間,若快速獲FDA批准,香港可透過「特別用藥計劃」或「 compassionate use」途徑引入,並由藥物名冊委員會評估成本效益,預計審批時間約12至18個月。 未來研究方向
Revolution Medicines正同步推進四項第三期註冊試驗,除RASolute 302外,尚包括RASolute 301(一線聯合吉西他濱與白蛋白紫杉醇)、RASolute 303(維持治療)及RASolute 203(非小細胞肺癌)。公司亦探索daraxonrasib與免疫檢查點抑制劑、SHP2抑制劑的聯用方案,初步臨床前數據顯示協同效應明顯,有望進一步擴大適應症至結直腸癌、子宮內膜癌等RAS依賴性腫瘤。 與此同時,Foundation Medicine與Guardant Health已開發出可檢測RAS G12突變的液體活檢套組,預計與daraxonrasib同步上市,簡化患者篩選流程。業界普遍關注即將於6月舉行的美國臨床腫瘤學會(ASCO)年會,屆時將公佈RASolute 302的完整數據與亞組分析,或進一步鞏固daraxonrasib在RAS靶向治療領域的先發地位。 對於長期缺乏突破的胰腺癌治療領域,daraxonrasib的13.2個月整體存活期數據是臨床的顯著進步,為患者與臨床醫生提供新選擇。隨著監管審批與商業化步伐加快,香港與亞太地區的高發病率人群有望於2027年起受益,讓「精準醫療」從實驗室走向病床的轉化。